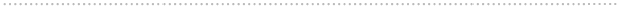光による環境に優しい新規な有機反応の開発
我々は、多種多様の有機分子の働きにより、現在の豊かな暮らしを享受している。例えば、医薬品・染料・香料などの有機分子が、それぞれの機能を果たすことで、我々の暮らしを向上させてくれる。しかし、これらの有機分子は、現在、環境に悪影響を及ぼす方法によって合成されており、より環境に優しい手法が求められている。このような背景のもと、光を利用した化学反応が最近注目されている。なぜなら、金属や加熱・加圧などを加えることなく、光を照射するだけで目的の有機分子を手に入れることができるからだ。このように、光を利用した有機化学反応は環境に優しく大きな可能性を秘めているが、光を有機分子に照射して生成する励起状態の反応性の高さゆえに、副反応や二次反応が起こりやすく、有機合成においては、収率よく目的物を得るのが困難であることが多い。我々は、これを克服するべく、有用な有機分子が合成できる新しい有機光反応の開発を行っている。具体的には、下に示す3つの有機光反応の研究を行っている。
研究テーマ
1)カルボン酸からの光脱炭酸を経由したラジカル反応
アミノ酸や脂肪酸に代表されるカルボン酸は、天然に広く存在し、重要な機能を有しているが、それらを様々な化合物へ化学変換する試みは大きな制限を受けている。それは、カルボン酸が有するカルボキシ基の脱炭酸 (脱カルボキシ化)を伴った官能基変換を温和な条件下で行うことが一般に困難であるためだ(Scheme 1)。
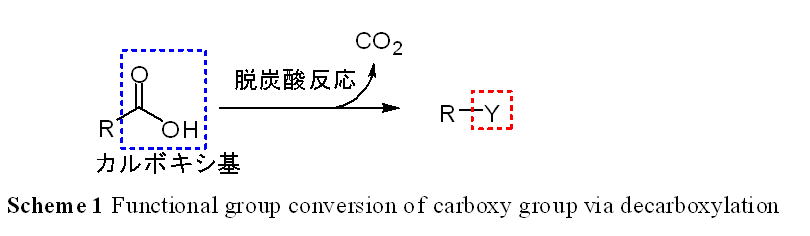
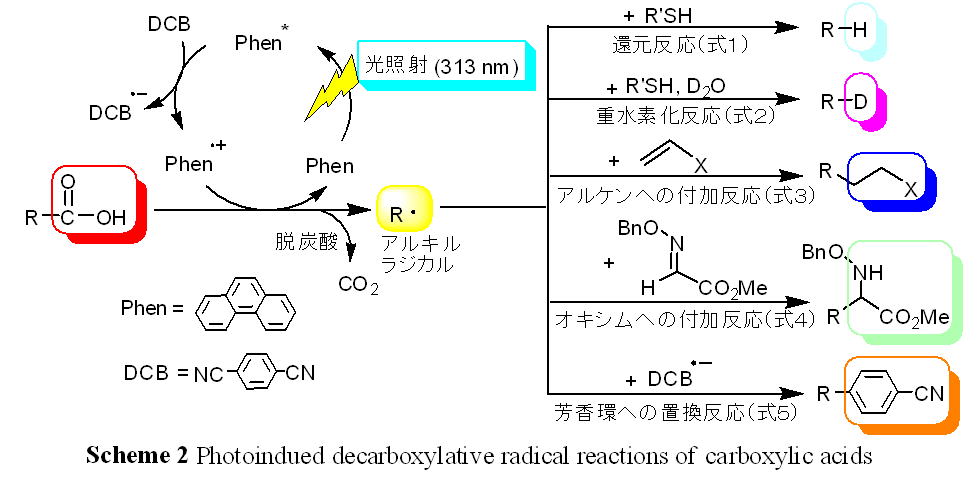
それらに対して、我々は、光誘起電子移動によって生じる芳香環のラジカルカチオンに脂肪族カルボン酸が酸化され、脱炭酸して、アルキルラジカルが生成することを見出した(Scheme
2)。この光反応では、光増感剤であるフェナントレン(Phen)が光を吸収して励起状態になり、電子アクセプター分子である1,4-ジシアノベンゼン(DCB)との間で光誘起電子移動反応が進行して、Phenのラジカルカチオンが生成する。カルボキシアニオンからラジカルカチオンに電子が移動し(酸化され)、カルボキシラジカルが生成した後、脱炭酸反応が起こり、アルキルラジカルを与える。この光反応の方法で生じるアルキルラジカルの濃度が低いため、ラジカルの二量化反応などの副反応が起こらず、チオールやアルケンなどと反応して、還元体や付加体を高収率で与える。このように、本光反応はフリーなカルボン酸から温和な条件下(室温・常圧)、金属などを使用せずに、アルキルラジカルを経由して、直接的なカルボキシ基の官能基変換ができる優れた特徴を有している。PhenやDCBは、他の光増感剤や電子アクセプター分子に置き換えることが可能であり、さらに、触媒量で充分であること、また、カルボン酸も1級から3級の脂肪族カルボン酸ならば基質として利用できるなど、光を駆動力とする一般性が高い触媒反応であるがわかった。
次に、この光脱炭酸を経由したラジカル反応の最近の研究成果を述べる(J. Org. Chem., 2013, 78, 582-589)。
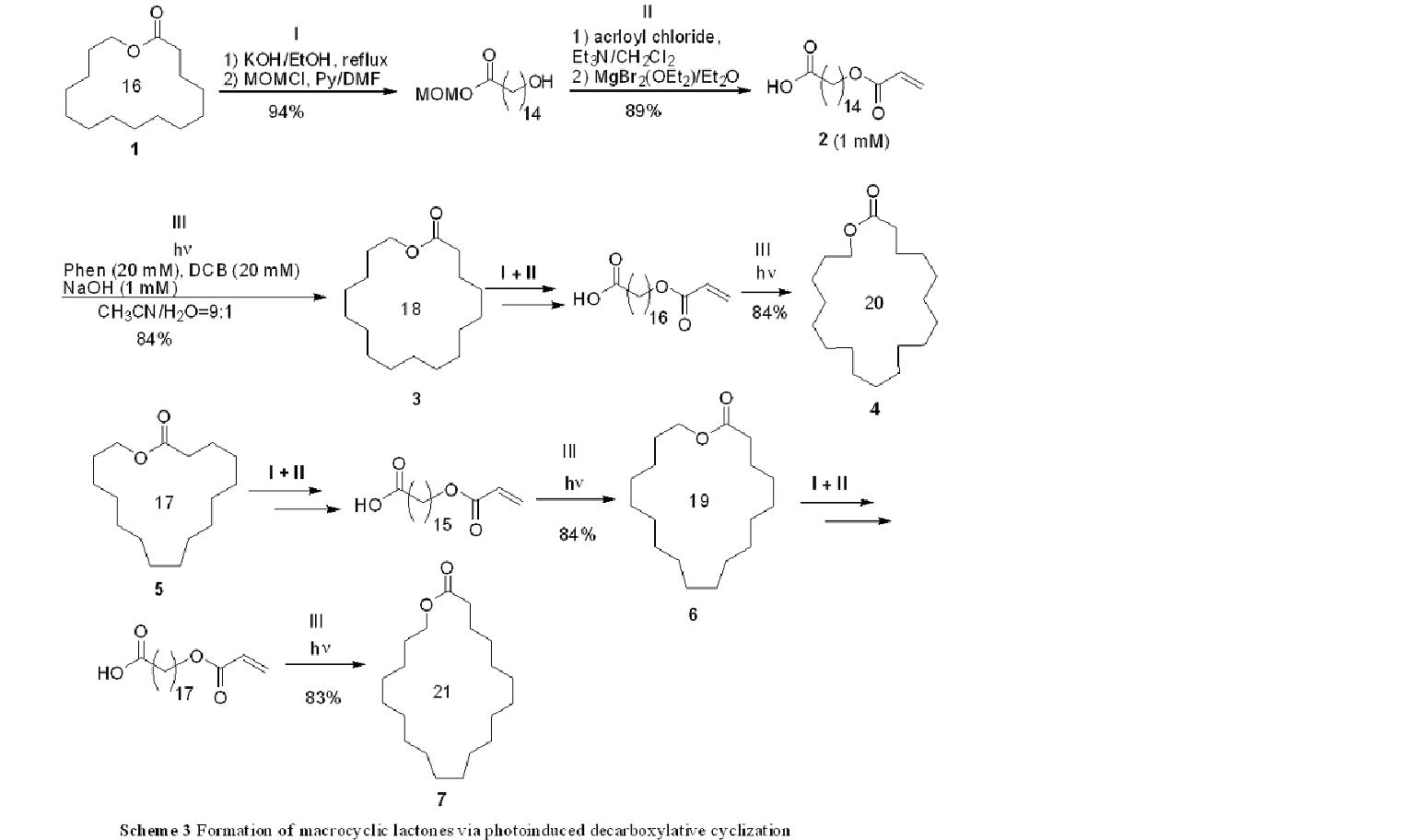
光脱炭酸経由のアルケンへの分子間付加反応が、アルケンを一当量用いるだけでも高収率で付加体を与えることに着目し、この光反応を分子内環化反応へ応用して、大環状ラクトン・ラクタム・ケトンの合成を検討した。16員環のラクトン 1 を加水分解し、カルボキシ基をMOM基で保護して(I)、ヒドロキシ基をアクリル酸クロライドと反応させ、MOM基を脱保護することで(II)、末端にカルボキシ基とアクリル酸エステルを有するカルボン酸 2 を合成した(Scheme
3)。高希釈条件下(1 mM)でカルボン酸2に光照射を行うと(III)、光脱炭酸を経由して、ラジカルが生成した後、分子内で環化し、高い収率(84%)で18員環の大環状ラクトン 3 を与えた。この18員環ラクトン3から、I, II, IIIの合成と光反応を行うことで、20員環の大環状ラクトン 4 が得られた。さらに、17員環ラクトン5から19員環ラクトン6、21員環ラクトン7もI, II, IIIの操作を繰り返すことで得ることができた。このように、光反応を含むこの方法を用いると、大環状ラクトンから二つの炭素鎖を拡張した大環状ラクトンが合成でき、これを繰り返すことで、望む炭素鎖の大環状ラクトンが得られる。
大環状ラクトンのエステル基を加水分解すればカルボキシ基とヒドロキシ基になり、そのカルボキシ基を本光反応で脱炭酸できるため、ヒドロキシ基をアミンもしくはアルキル基にすれば、大環状ラクタム・ケトンが合成できると考えた。16員環のラクトン
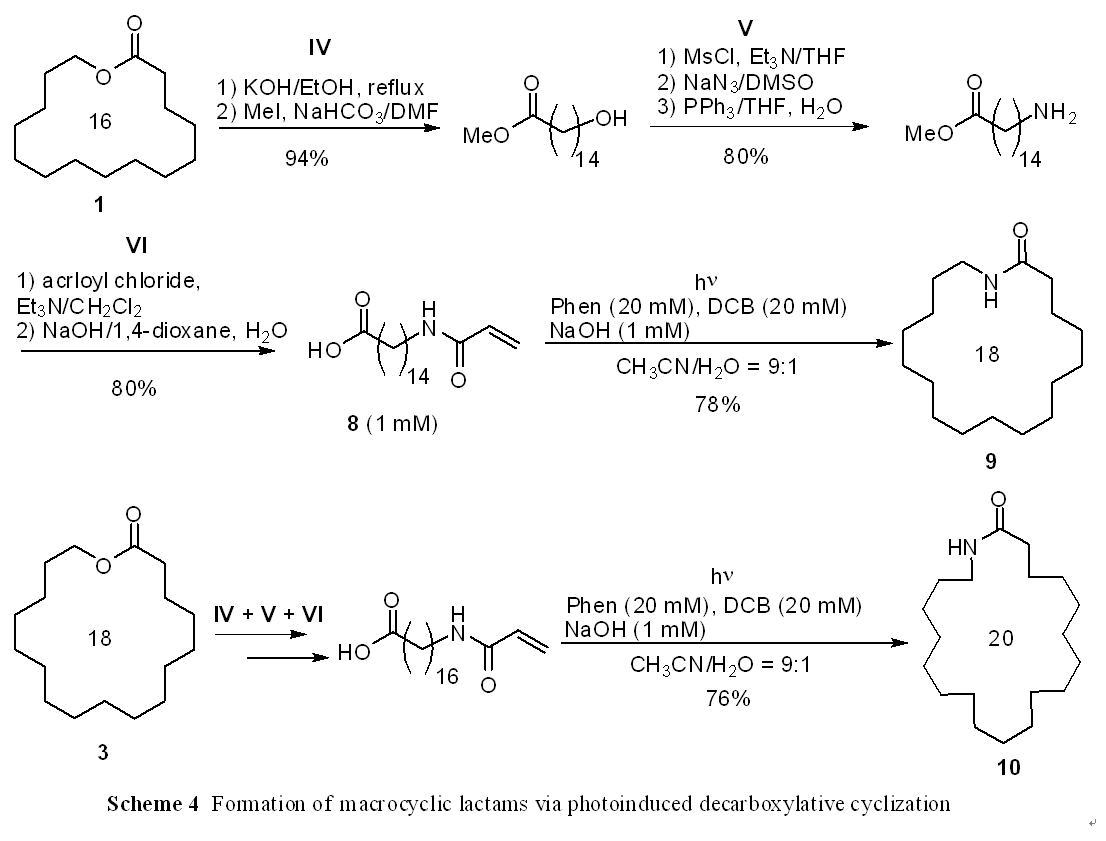
1 を加水分解し、カルボキシ基をメチルエステルにした後(IV)、ヒドロキシ基をアミンに変換し(V)、アクリル酸クロライドと反応させ、メチルエステルを加水分解することで(VI)、末端にカルボキシ基とアクリル酸アミドを有するカルボン酸
8 を合成した(Scheme 4)。同様に、高希釈条件下(1 mM)、この光反応を行うと、脱炭酸を経由して、分子内で環化し、18員環の大環状ラクタム
9 が収率よく得られた。さらに、IV, V, VIの合成と光反応を行うことで、18員環の大環状ラクトン3から20員環の大環状ラクタム 10 が得られた。このように、この手法を用いることで、大環状ラクトンから二つの炭素鎖が拡張した大環状ラクタムが合成できる。
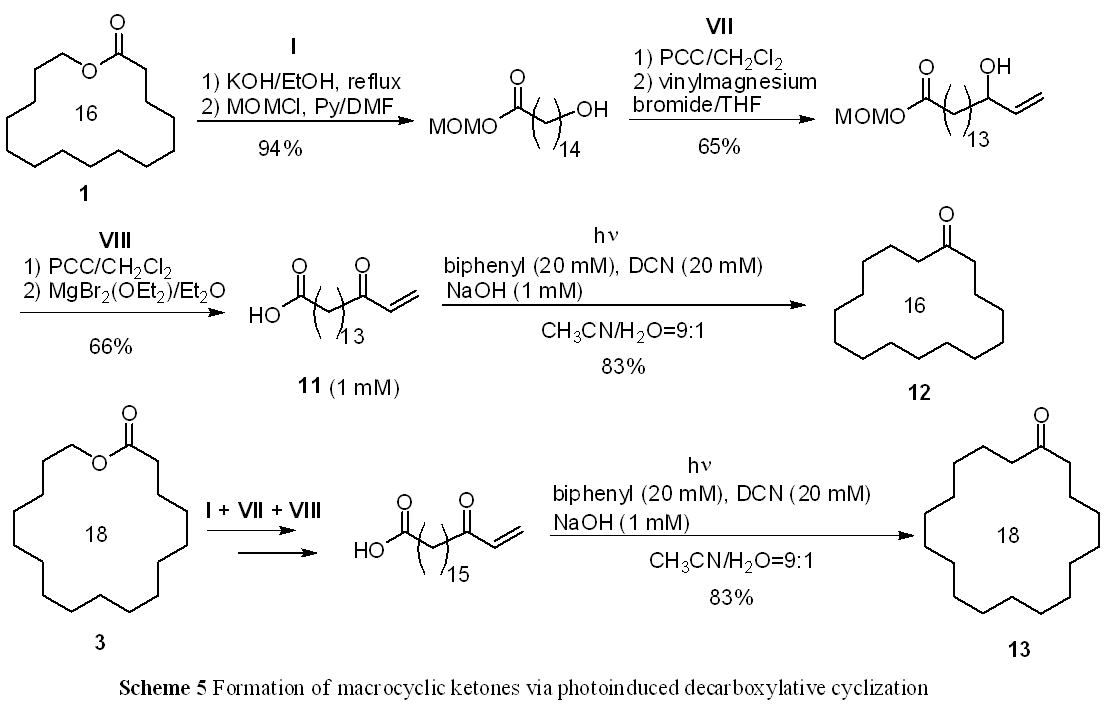
次に、この光反応による大環状ケトンの合成を検討した。16員環ラクトン1から加水分解、MOM基で保護を行い(I)、アルコールをPCCで酸化した後、ビニルマグネシウムブロマイドと反応させ(VII)、PCCによる酸化と脱保護で(VIII)、末端にカルボキシ基と,-不飽和ケトンを有するカルボン酸11を合成した(Scheme 5)。ここでは、Phenの代わりにビフェニルを、DCBの代わりに1,4-ジシアノナフタレン(DCN)を用いて11の光反応を行うと、高収率で16員環の大環状ケトン12を得ることに成功した。同様に、I, VII, VIIIの操作と光反応を行うことで、18員環の大環状ラクトン3から18員環の大環状ケトン 13 が得られた。このように、この手法により大環状ラクトンから同じ炭素鎖数の大環状ケトンが合成できる。
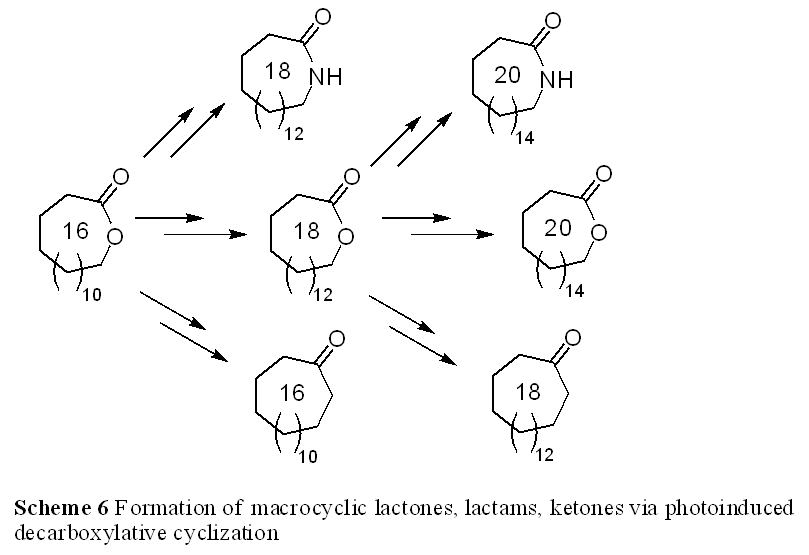
これら一連の光反応を用いた大環状化合物の合成により、大環状ラクトンから、2つの炭素鎖数が増えた大環状ラクトンが合成でき、さらに、2つの炭素鎖数が増えた大環状ラクタムが合成でき、また、同じ炭素鎖数の大環状ケトンが合成できることを明らかにした(Scheme
6)。途中の合成過程が長いため、多数の置換基を有する化合物には保護などの必要性が考えられるが、この手法を用いることで、大環状ラクトンから様々な炭素鎖数の大環状ラクトン・ラクタム・ケトンの合成が可能である。
2)ヒドロキシアニオンを電子ドナーとする光誘起電子移動反応
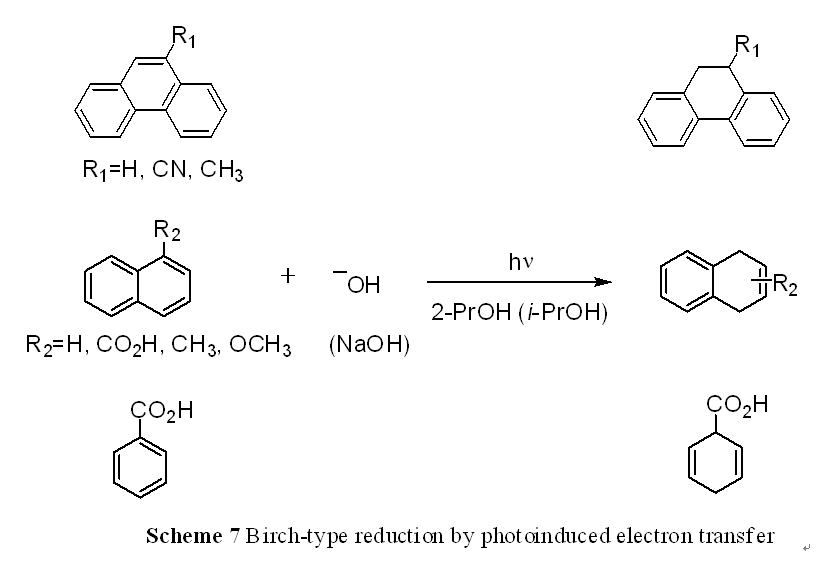
安定な構造である芳香環を壊すためには、非常に反応性が高く危険な試薬を用いる必要がある。例えば、芳香環を還元できる反応としてBirch還元が知られており、液体アンモニア中、爆発性の危険がある金属ナトリウムや金属リチウムを電子ドナーとして用いる。このように、反応性が高い試薬や厳しい反応条件が必要であるため、複数の官能基を有する有機分子では使用できず、人体や環境への悪影響も懸念される。これに対して、我々は、光励起させた芳香環に対し、ヒドロキシイオンが電子ドナーとして働くことを見出した(Scheme
7)。この光反応では、ナトリウムやリチウムといった危険な金属を使用することなく、室温下、2-プロパノール溶媒中、NaOHを加え光照射するだけで、フェナントレンやナフタレン、ベンゼンなどの芳香環の還元反応が進行することを明らかにした。
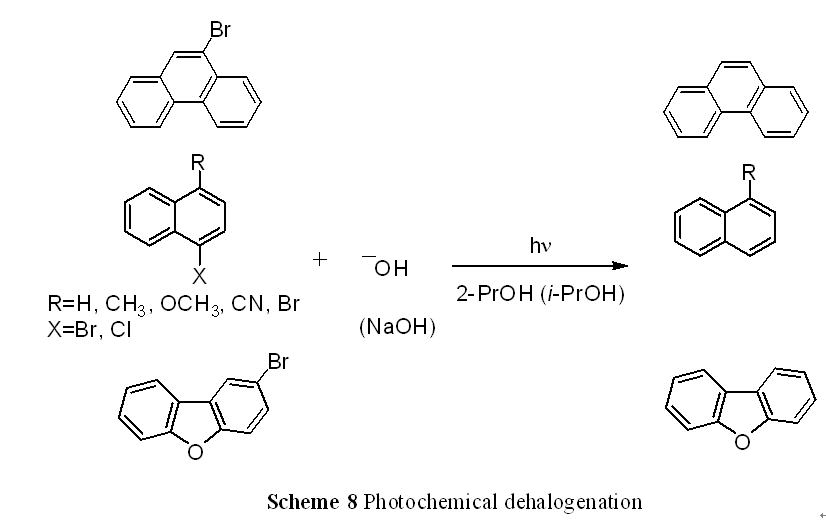
さらに、この光反応を脱ハロゲン化に応用した。ハロゲンが芳香環に直接結合したハロアレーンに、同様な条件下、光照射すると脱ハロゲン化が高収率で進行した(Scheme 8)。
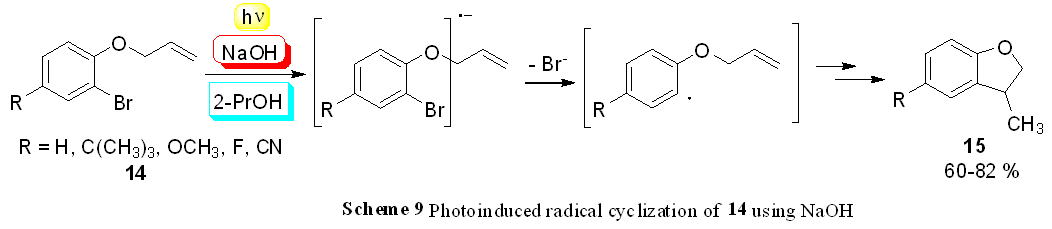
また、この光脱ハロゲン化では、途中にアレーンラジカルが生成するので、このラジカルを利用した環化反応を検討した。2位にブロモ基を有するアリールアリルエーテル14に、2-プロパノール中、NaOHを加え、光照射するだけで、脱ハロゲン化、続くラジカル環化反応が進行して5員環の生成物15を高収率で得ることができた(Scheme
9)。従来の方法では、環境に有害な(Bu)3SnHやAIBNを使用して、加熱する必要があったが、この光反応ではNaOHを加え光照射するだけでよいため、環境に優しい方法である。
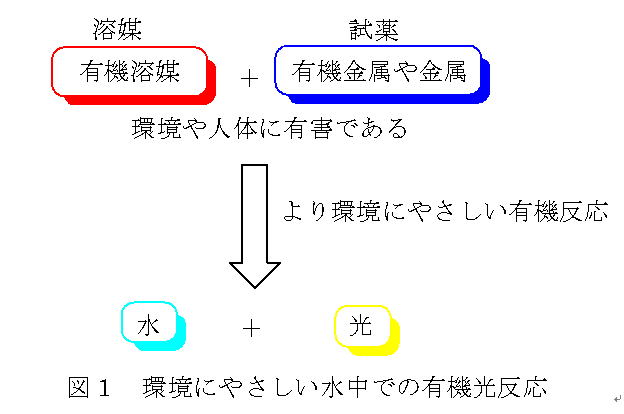
有用な有機分子を合成するときに多量に使用するものが、トルエンやエーテル、アルコールなどの有機溶媒である。しかし、有機溶媒は人体や環境にとって有害であり、爆発や発火の危険性が大きいので、その使用をなるべく避けなければいけない。さらに、これらの合成過程では、環境に悪影響を及ぼす有機金属や金属も試薬として用いている。つまり、有機分子の製造で使われている有機溶媒と金属を、より環境に優しいものへと変換する必要がある。このような背景から、我々は水を溶媒として、光を用いた環境調和型有機反応の開発を行っている(図1)。水は、発火の危険性はなく、環境に対してまったく負荷のない物質であり、さらに、光は金属とは違い反応終了後、系中に残存せず、しかも、強力に反応を進行させることができる。このように、水中での光を用いた有機反応を行うことができれば、環境への負荷を大きく減らすことができる。
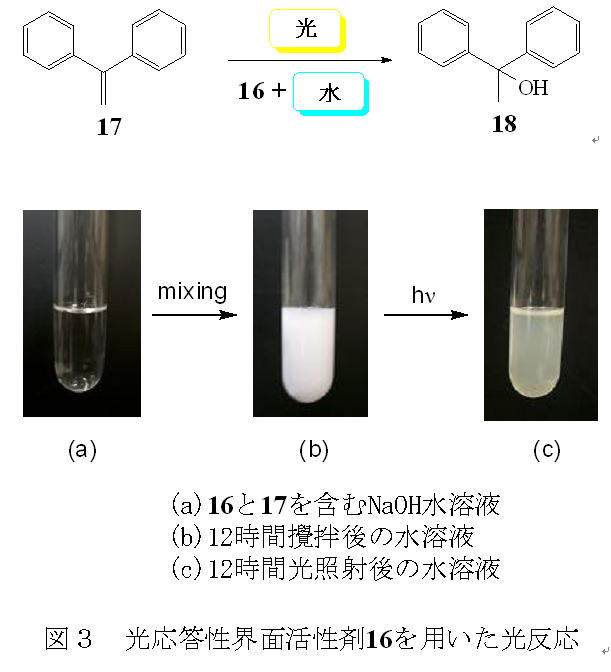
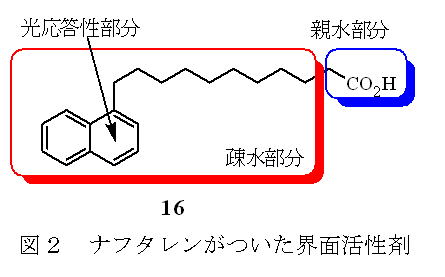
しかし、水を溶媒として用いた有機反応の大きな問題点として、有機分子は水に不溶であるために、水中では反応が進行しないことである。これを解決する方法として、水と油(有機分子)を混ぜ合わすことができる界面活性剤(せっけん)の性質に着目した。末端にナフタレンなどの光を吸収できる発色団を連結した界面活性剤16を合成し、これを水中での光反応に用いた(図2)。実際の反応例を次に示す。
界面活性剤 16 と水に溶解しないジフェニルエテン 17 を水中で12時間撹拌すると、白く濁ったエマルション溶液(洗剤を入れた洗濯機の中で油汚れがひどい洋服を洗った水のような状態)が得られる(図3(b)の溶液)。このエマルション溶液に光照射すると、ジフェニルエテンに水が付加したアルコール 18 が高収率で得られた。このように、水に溶解しない有機分子でも、16のような界面活性剤を加えることにより水中での光反応が可能になった。これらの界面活性剤は反応終了後、回収でき、繰り返し使用できるので、廃棄物を出さずに、有機溶媒も使用せずに反応が行える。